Gốc axit là gì? Đây là thuật ngữ khá quen thuộc trong các môn học hóa học và các lĩnh vực nghiên cứu hóa chất hay sức khỏe. Tuy nhiên, không phải ai cũng có thể nhớ rõ, hiểu sâu và vận dụng tốt các kiến thức về axit
Cùng Kangaroo ôn lại những kiến thức hóa học cũ về gốc axit, phân loại và tính chất của gốc axit trong nội dung bài viết dưới đây nhé!
Gốc axit là gì ?
Gốc axit là một phần trong phân tử axit khi thực hiện tách nguyên tử Hidro linh động trong phân tử.
Ví dụ:
- Axit HCl tách nguyên tử Hiđro thì thu được gốc axit -Cl
- Axit HNO3 tách nguyên tử Hiđro thì thu được gốc axit -NO3
- Axit H2SO4 tách nguyên tử Hiđro thì thu được gốc axit =SO4 hoặc -HSO4
- Axit H3PO4 tách nguyên tử Hiđro thì thu được gốc axit ☰PO4 hoặc =HPO4 hoặc -H2PO4
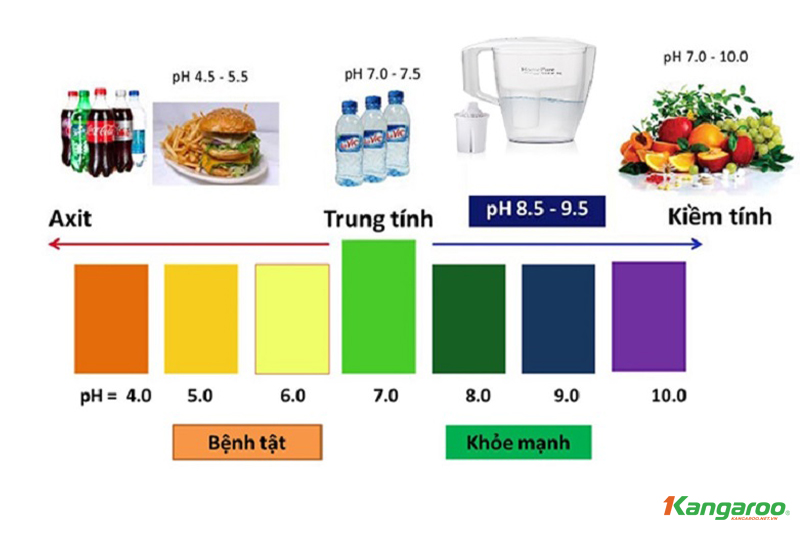
Ngoài được nghiên cứu trong các phòng thí nghiệm, môn hóa học tại nhà trường thì chúng ta còn có thể tìm được gốc axit trong nước uống hàng ngày khi chưa qua các hệ thống lọc, các loại thực phẩm hàng ngày có axit như cam, chanh, một số loại hoa quả khác,...
Phân loại gốc axit gồm những gì?
Dựa theo cấu tạo, người ta phân gốc axit thành 2 loại là gốc axit có Hidro và gốc axit không có Hidro:
- Gốc axit có Hidro: -HSO4, =HPO4, -H2PO4
- Gốc axit không có Hidro: -Cl, -NO3, =SO4, ☰PO4
Ngoài ra, người ta còn phân loại gốc axit thành gốc axit có oxi và gốc axit không có oxi:
- Gốc axit có oxi: -NO3, =SO4, ☰PO4
- Gốc axit không có oxi: -Cl, -Br, -F, -I
Để bạn đọc có thể hiểu rõ hơn về axit, gốc axit tương ứng và cách gọi tên từng gốc axit, tham khảo ngay bảng dưới đây:
|
Axit và gốc axit |
|||||||
|
STT |
Công thức axit |
Tên gọi Axit |
Khối lượng axit (đvC) |
Công thức gốc axit |
Tên gọi gốc axit |
Hóa trị |
Khối Lượng Gốc Axit (đvC) |
|
1 |
HCl |
Axit clohidric |
36.5 |
-Cl |
Clorua |
I |
35.5 |
|
2 |
HBr |
Axit bromhidric |
81 |
-Br |
Bromua |
I |
80 |
|
3 |
HF |
Axit flohidric |
20 |
-F |
Florua |
I |
19 |
|
4 |
HI |
Axit iothidric |
128 |
-I |
Iotdua |
I |
127 |
|
5 |
HNO3 |
Axit nitric |
63 |
-NO3 |
Nitrat |
I |
62 |
|
6 |
HNO2 |
Axit nitric |
47 |
-NO2 |
Nitrit |
I |
46 |
|
7 |
H2CO3 |
Axit cacbonic |
62 |
=CO3 |
Cacbonat |
II |
60 |
|
-HCO3 |
Hidrocacbonat |
I |
61 |
||||
|
8 |
H2SO4 |
Axit sunfuric |
98 |
=SO4 |
Sunfat |
II |
96 |
|
-HSO4 |
Hidro Sunfat |
I |
97 |
||||
|
9 |
H2SO3 |
Axit sunfuric |
82 |
=SO3 |
Sunfit |
II |
80 |
|
-HSO3 |
Hidro Sunfua |
I |
81 |
||||
|
10 |
H3PO4 |
Axit photphoric |
98 |
PO4 |
Photphat |
III |
95 |
|
-H2PO4 |
Dihydro Photphat |
I |
97 |
||||
|
=HPO4 |
Hidro Photphat |
II |
96 |
||||
|
☰PO4 |
Photphat |
III |
95 |
||||
|
11 |
H3PO3 |
Axit photphoric |
82 |
☰PO3 |
Photphat |
III |
79 |
|
-H2PO3 |
Đihiđrophotphit |
I |
81 |
||||
|
=HPO3 |
Hidrophotphat |
II |
80 |
||||
|
12 |
H2SO3
|
Axit Sunfit
|
82
|
=SO3 |
Sunfit |
II |
80 |
|
-HSO3 |
Hidro sunphit |
I |
81 |
||||
|
13 |
H2CO3
|
Axit Cacbonic |
62 |
=CO3 |
Cacbonat |
II |
60 |
|
-HCO3 |
Hidrocacbonat |
I |
61 |
||||
|
14 |
H2S |
Axit Sunfuhiđric |
34 |
=S |
Sunfua |
II |
32 |
|
-HS |
Hidro Sunfua |
I |
33 |
||||
|
15 |
H2SiO3 |
Axit silicic |
78 |
=SiO3 |
Silicat |
II |
76 |
|
-HSiO3 |
Hidro Silicat |
I |
77 |
||||
Tính chất hóa học của axit
Axit làm đổi màu quỳ tím thành màu đỏ và phản ứng với kim loại, bazo, oxit bazo và muối, cụ thể:
- Tác dụng với kim loại tạo ra muối: Axit + Kim loại → Muối + H2
Điều kiện phản ứng:
- Axit là axit loãng
- Kim loại đứng được Hidro trong dãy hoạt động hóa học
Ví dụ:
2Na + 2HCl → 2NaCl + H2
2Fe + 6H2SO4 → 3SO2 + Fe2(SO4)3 + 6H2O
- Tác dụng với bazo tạo ra muối: Axit + Bazo → Muối + H2O (phản ứng trung hòa)
NaOH + HCl → NaCl + H2O
Ba(OH)2 + 2HCl → BaCl2+ 2H2O
- Tác dụng với oxit bazo tạo muối: Axit + Oxit Bazo → Muối + H2O
Na2O + 2HCl → 2NaCl + H2
CuO + 2HCl → CuCl2 + H2O
- Tác dụng với muối
Điều kiện phản ứng:
- Sau phản ứng tạo ra kết tủa hoặc khí bay hơi
- Nếu thu được muối tan thì axit thu được là axit yếu. Còn nếu thu được muối không tan thì axit thu được là axit mạnh.
Ví dụ:
H2SO4 + BaCl2 → BaSO4(r) + 2HCl
K2CO3 + 2HCl → 2KCl + H2O + CO2 (H2CO3 phân hủy ra H2O và CO2)
Ứng dụng của một số axit
Axit được ứng dụng trong rất nhiều các hoạt động của đời sống hàng ngày, đóng vai trò không thể thay thế:
- Lĩnh vực công nghiệp: Axit được sử dụng để loại bỏ các gỉ sắt, làm sạch bề mặt trước khi hàn, sử dụng để làm chất điện phân trong pin xe hơi, bình acquy; sản xuất phân bón, điều chế các chất tẩy rửa, điều chế dầu mỏ, muối và axit, thuốc nổ, luyện kim, điều chế chất dẻo, tẩy trắng giấy,...
- Lĩnh vực thực phẩm: Axit được sử dụng vô cùng phổ biến: làm chất tạo màu, điều chỉnh độ chua, chất chống tạo bọt, chất chống vón, chất chống oxy hóa, chất tạo lượng, giữ màu, chất chuyển thể sữa, điều vị, tạo vị, xử lý bột ngũ cốc, giữ ẩm, chất ổn định,...
- Lĩnh vực dược phẩm: Aspirin là một loại thuốc có chứa axit được sử dụng để giảm sốt đã được nghiên cứu từ cuối thế kỷ 19
- Trong cơ thể người axit đóng vai trò vô cùng quan trọng giúp tiêu hóa thức ăn bằng cách phá vỡ các phân tử thức ăn có cấu trúc phức tạp, tổng hợp các Protein cần thiết cho sự phát triển, sửa chữa các mô trong cơ thể.
Đồng thời, các axit nucleic cũng rất cần thiết cho việc sản xuất DNA, RNA và chuyển các đặc tính sang con lai qua gen.
Ngoài ra, axit cacbon còn có đóng nhiệm vụ quan trọng trong duy trì và cân bằng độ pH trong cơ thể.
Tuy nhiên, người sử dụng cần cẩn trọng đối với axit và các chế phẩm từ axit bởi nó có thể gây ra những tai nạn đáng tiếc - bỏng axit nghiêm trọng, làm biến dạng các bộ phận cơ thể, thậm chí là tử vong.
Chính vì thế, khi sử dụng axit, chúng ta cần tuân thủ các phương pháp bảo hộ như đeo găng tay, mặc quần áo bảo hộ, đeo khẩu trang, không mở pipet bằng miệng, tuân thủ hướng dẫn sử dụng,...
Trong quá trình lưu trữ axit lưu ý: không lưu trữ axit bằng thùng kim loại bởi axit có thể ăn mòn bình chứa, đậy nắp kín đáo, để nơi khô ráo, tránh ánh nắng trực tiếp, tránh bảo quản chung với các chất có tính axit để hạn chế cháy nổ nghiêm trọng.
Trên đây là những thông tin giải đáp gốc axit là gì, phân loại, tính chất và ứng dụng của gốc axit trong các lĩnh vực của đời sống. Cảm ơn bạn đọc đã dành thời gian theo dõi bài viết của Kangaroo ! Chúng tôi còn cung cấp thêm máy lọc nước kangaroo đảm bảo sức khỏe bạn có thế tham khảo cho gia đình .









